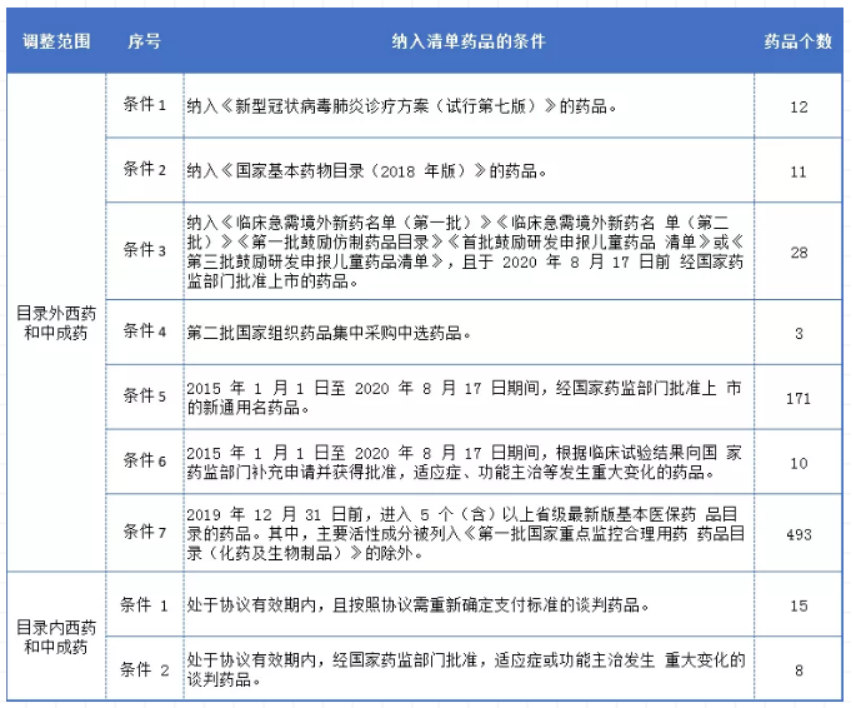
9月18日,國家醫(yī)保局公示《2020年國家醫(yī)保藥品目錄調(diào)整通過形式審查的申報藥品名單》,據(jù)統(tǒng)計,此次發(fā)布通過形式審查的藥品約在751種(因符合不同申報情形,部分品種有重復)。涉及化藥573種,中藥178個。其中,包括18個醫(yī)保目錄內(nèi)產(chǎn)品,主要為協(xié)議期滿需重新確定支付標準以及擴展適應證的品種;其余均為目錄外品種,目錄外西藥和中成藥形式審查的條件共有7個(滿足其中一個即可)。
2020年國家醫(yī)保藥品目錄調(diào)整納入名單藥的條件及藥品個數(shù)
名單看點十足,“GV-971”納入醫(yī)保合適否?
本次國家醫(yī)保局發(fā)布2020年醫(yī)保目錄初審名單,看點十足:此次通過形式審查的藥品名單中,2019年12月31日前,進入5個(含)以上省級最新版基本醫(yī)保藥品目錄的藥品有493個,占審查通過藥品名單的2/3,為納入的最多的一類藥品;其次引人注目的是2015年之后獲批的創(chuàng)新藥,最有代表和最火熱的品種當屬于PD-1/PDL-1,本次有7個納入名單之中,除已納入醫(yī)保的達伯舒外,目前在中國上市的所有PD-1/PDL/1全部入圍;此外還有讓人意想不到的是,此前備受爭議的阿爾茨海默病新藥GV-971也入選本次名單之列。
GV-971我國自主研發(fā)并擁有自主知識產(chǎn)權(quán)的創(chuàng)新藥,是在全球各大制藥公司投入數(shù)千億美元研發(fā)均告失敗、全世界17年來無阿茲海默癥新藥獲批的背景下,我國國家藥監(jiān)局有條件的批準了該藥品的上市,然引發(fā)了網(wǎng)友對該藥品“靠譜”的質(zhì)疑,現(xiàn)又出現(xiàn)在醫(yī)保目錄初審名單之列,再次引發(fā)網(wǎng)友熱議,不禁讓人發(fā)問,GV-971納入醫(yī)保合適否?
藥智藥聯(lián)合創(chuàng)始人李天泉表示,實際上GV-971納入醫(yī)保可以從兩個不同的角度看:
一方面,GV-971為國家新批上市的具有完全自主、全球首創(chuàng)的創(chuàng)新藥,從保護企業(yè)對創(chuàng)新藥開發(fā)的積極性,鼓勵創(chuàng)新角度而言,GV-971是完全有資格被納入醫(yī)保之內(nèi),且全球阿爾茨海默病患者均期盼能夠有更多針對阿爾茨海默癥治療的有效新藥出現(xiàn)。
另一方面,GV-971的批準上市受到很多專家的質(zhì)疑,首都醫(yī)科大學校長、原北京大學生命科學學院院長饒毅就曾發(fā)文質(zhì)疑GV-971的“效用問題”,認為“GV-971”的“多靶點”效用存在夸大嫌疑。同時指出,“GV-971”的研究團隊耿美玉此前已發(fā)表了12篇與“GV-971”相關或密切相關的論文,然而,耿美玉及其團隊在2019年發(fā)布的“GV-971”論文中并未引用其中的任何一篇。此種情況下,過早的將GV-971納入醫(yī)保值得討論,畢竟GV-971的上市是國家藥監(jiān)局“有條件批準”的,“有條件”就是國家藥監(jiān)局要求申請人上市后繼續(xù)進行藥理機制方面的研究和長期安全性、有效性研究,完善寡糖的分析方法,按時提交有關試驗數(shù)據(jù),如果將來沒有得到進一步的數(shù)據(jù)支持,那么這個藥物批準就會被撤回。也就意味著該藥的臨床效果還需進一步的得到100%的有效驗證,如果后期該藥品臨床反應良好,取消掉“有條件”批準后再納入醫(yī)保,應當是最穩(wěn)妥的一種方式。
重點監(jiān)控輔助用藥與OTC納入,是否有違前期規(guī)則?
今年7月31日,國家醫(yī)保局發(fā)布的《基本醫(yī)療保險用藥管理暫行辦法》第三十六條明確規(guī)定,原則上《藥品目錄》不再新增OTC藥品。然而此次公示的名單之中仍有不少OTC的品種被列入,如:藿香正氣合劑、牛黃清感膠囊、鼻康片、鼻通滴鼻劑等藥品。
另在醫(yī)保藥品的動態(tài)調(diào)整,在調(diào)出的藥品中,重點監(jiān)控名單內(nèi)的藥品是被重點關注的對象,形式審查通過的名單中也有輔助用藥和重點監(jiān)控用藥,以及2019年被踢出醫(yī)保的藥品在內(nèi),名單十分復雜,由此引發(fā)網(wǎng)友的爭議,發(fā)問“是否違背了前期原則?”
同時,有行業(yè)專家指出,本次調(diào)入名單符合第五個條件的藥品依達拉奉右莰醇注射用濃溶液及依達拉奉氯化鈉注射液,雖然依達拉奉右莰醇注射用濃溶液為化藥1類,屬于創(chuàng)新藥類,但是依達拉奉右莰醇注射用濃溶液及依達拉奉氯化鈉注射液兩藥品的主要活性成分還是依達拉奉,而依達拉奉注射劑屬于重點監(jiān)控,理論上不應被納入醫(yī)保目錄。
也有專家指出,依達拉奉右莰醇注射用濃溶液及依達拉奉氯化鈉注射液雖然主要成分是依達拉奉,但一個藥品進入醫(yī)保形式審查名單或者說納入醫(yī)保目錄,是以單個藥品品種通過醫(yī)保形式審查或醫(yī)保審查后被列入,而非看的是一個品種的主要成分。
依達拉奉右莰醇注射用濃溶液為化藥1類,為先聲藥業(yè)的獨家品種,且是按照優(yōu)先審評和特殊審評獲批上市的,說明該藥品符合臨床急需用藥,同時符合2015年1月1日至2019年12月31日期間,經(jīng)國家藥監(jiān)部門按新藥注冊申請程序批準上市的藥品(包括新活性成分、新劑型)規(guī)則,納入名單之列是沒有問題的。
此外,依達拉奉氯化鈉注射液是按照新化藥注冊分類3類獲批上市,雖然依達拉奉被納入輔助用藥和重點監(jiān)控藥品目錄,但是依達拉奉氯化鈉注射液獲批上市的企業(yè)較少,目前僅江蘇正大豐海于2019年年末獲批上市,在依達拉奉注射劑被重點監(jiān)控之前是沒有依達拉奉氯化鈉注射液品種的,因此依達拉奉氯化鈉注射液進入醫(yī)保形式審查名單之列存在一定的合理性,但是我們需要做的是對于依達拉奉氯化鈉注射液的合理跟蹤,一旦藥品用量過高或出現(xiàn)嚴重不良反應,那么就應該被限制使用。
根據(jù)《2020年國家醫(yī)保藥品目錄調(diào)整工作方案》,醫(yī)保目錄調(diào)整時間安排分為五個階段:準備階段(2020年7-8月)、申報階段(2020年8-9月)、專家評審階段(2020年9-10月)、談判和競價階段(2020年10-11月)和公布結(jié)果階段(2020年11-12月)。目前公布的醫(yī)保調(diào)整藥品初審名單,為遴選目錄,緊接著馬上會進入藥學(含藥物經(jīng)濟學)、臨床醫(yī)學及醫(yī)保專家審評階段。2020年醫(yī)保初審內(nèi)藥品如若順利通過專家審評,進入醫(yī)保談判階段,對于醫(yī)藥企業(yè)而言又將是一次“大考”。同時公示的751個藥品,本身復雜程度就頗受爭議,后期又會面臨降價談判,到底會有多少品種笑到最后,成功入圍?拭目以待。
聲明:本文觀點僅代表作者本人,本文來源于藥智網(wǎng)三七,歡迎在留言區(qū)交流補充
