本期(8月14日至8月21日)國際、國內市場風起云涌,幾家歡喜幾家愁。在國際上,諾華PI3K抑制劑Piqray (alpelisib)在加拿大獲批上市,聯合氟維司群(fulvestrant)用于治療接受內分泌療法后病情進展、PIK3CA突變、HR+/HER2-局部晚期或轉移性乳腺癌女性(絕經后)和男性患者。FDA批準羅氏創新IL-6抑制劑上市,治療視神經脊髓炎譜系障礙;吉利德JAK抑制劑類風濕性關節炎(RA)適應癥美國上市申請遭拒;BioMarin血友病基因治療遭FDA拒絕批準。
在國內,第三批國采如火如荼進行,跨國原研企業抱團棄標,國內仿制企業競爭激烈。而本期NMPA又批準多個仿制藥上市,紅海競爭加劇,更多動態如下:
國內審評審批·新動態
本周CDE有58個受理號(41個品種)報生產辦理狀態更新,其中東陽光、科倫藥業多個品種獲批,司太立碘克沙醇、復宏漢霖曲妥珠單抗備受關注,更多動態如下:
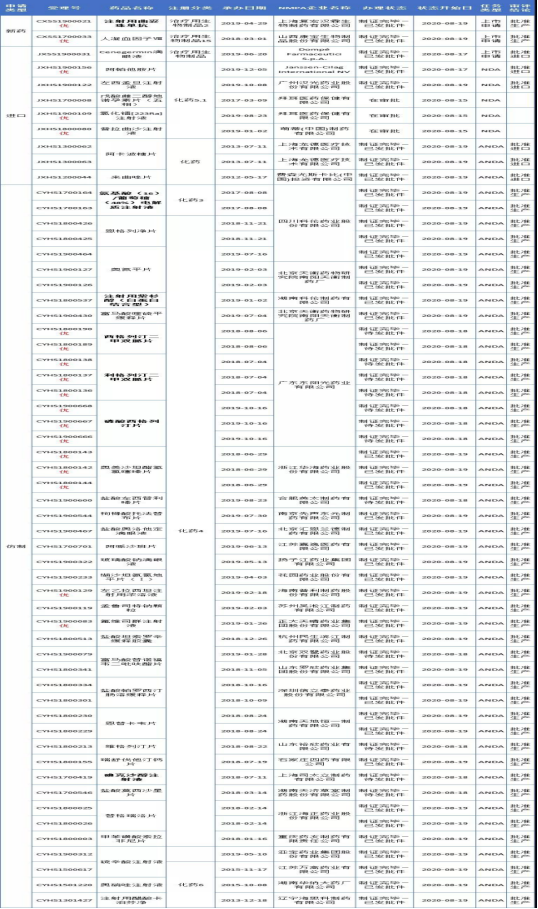
東陽光糖尿病領域再添3款重磅品種
8月18日,廣東東陽光藥業3款以仿制4類申報的糖尿病產品獲批上市,在降糖領域一連獲多款重磅品種。其中西格列汀二甲雙胍片和利格列汀二甲雙胍片為首仿,磷酸西格列汀片是國內獲批的第二家企業,首仿為正大天晴。
利格列汀二甲雙胍片是勃林格殷格翰/禮來聯合研發的DPP-4抑制劑利格列汀與二甲雙胍組成的復方口服降糖藥,2019年全球銷售額為15.59億歐元。西格列汀二甲雙胍片是默沙東研發的DPP-4抑制劑西格列汀與二甲雙胍組成的復方口服降糖藥,2019年全球銷售額為20.41億美元。藥智數據顯示,在糖尿病領域,東陽光此前已有重組人胰島素注射液和4 類仿制藥利格列汀片獲批上市,此次又有利格列汀二甲雙胍片、磷酸西格列汀片和西格列汀二甲雙胍片獲批上市,其糖尿病產品管線得到進一步豐富。
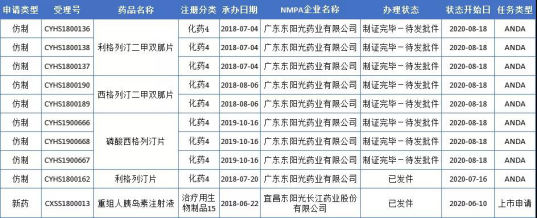
科倫藥業多款產品獲批上市
近日,科倫藥業奧氮平片、恩格列凈片、注射用紫杉醇(白蛋白結合型)、復方氨基酸/葡萄糖電解質注射液4款產品獲得藥品注冊批件。
復方氨基酸(16AA-Ⅱ)/葡萄糖(48%)電解質注射液為貝朗開發的腸外營養雙室袋,臨床適用于口服或腸內營養無法進行、不足或禁忌時,為中重度分解 代謝患者提供腸外營養治療所需的氨基酸、葡萄糖等營養成分。目前該產品原研尚未進口,科倫為國內首家批準上市。
注射用紫杉醇(白蛋白結合型)由新基公司開發,獲批用于治療乳腺癌、肺癌和胰腺癌。2019年本品中國銷售額已達44.4億元。2020年3月,國家藥品監督管理局在對新基公司開展藥品境外生產現場檢查后,宣布因該產品部分關鍵生產設施不符合我國藥品生產質量管理的基本要求,暫停其在中國進口、銷售和使用。目前,該品種獲批的國內廠家有石藥、恒瑞和齊魯制藥。
奧氮平片為禮來開發的非典型抗精神病藥,用于治療精神分裂、 中到重度躁狂發作及預防雙相情感障礙復發。奧氮平為中國臨床最常用的一線抗精神病藥物之一,2019年奧氮平片中國公立醫院銷售額約 40.7億元,占抗精神病藥物總銷售額的39.6%。
恩格列凈片為勃林格殷格翰和禮來共同開發的鈉-葡萄糖共轉運蛋白2抑制劑(SGLT2i),2019年全球銷售額高達49億美元。據悉,恩格列凈片為科倫首個獲批進入糖尿病領域的藥物,未來將與公司已申報的卡格列凈片、西格列汀片等及在研的多個新型降糖藥,共同形成糖尿病領域產品集群。
首個新4類碘克沙醇注射液獲批上市,司太立強勢進軍造影制劑端
8月18日,司太立新4類仿制藥碘克沙醇注射液獲批上市,成為該品種國內首家通過一致性評價的產品。碘克沙醇由GE Healthcare AS(通用電氣)開發,是一種X-線造影劑,2019年中國公立醫療機構終端碘克沙醇注射液銷售額超過35億元。
司太立是國內造影劑原料藥龍頭,目前,司太立已經向CDE提交碘海醇注射液、碘帕醇注射液、碘克沙醇注射液、碘佛醇注射液、碘美普爾注射液等5款造影劑的上市申請。其中,碘帕醇注射液、碘海醇注射液已先后獲批并視同過評,碘克沙醇注射液成為司太立第三款造影劑制劑產品。

復宏漢霖曲妥珠單抗中國獲批上市
近日,復宏漢霖自主開發和生產的曲妥珠單抗漢曲優?獲批上市,成為首個國產曲妥珠單抗生物類似藥。7月27日,該藥已獲歐盟委員會批準上市,成為首個中歐雙批的國產單抗生物類似藥。漢曲優?獲得原研在中國已獲批準的所有適應癥:1)HER2陽性早期乳腺癌;2)HER2陽性轉移性乳腺癌;3)HER2陽性轉移性胃癌。曲妥珠單抗已于2017年被納入國家醫保目錄。漢曲優?的獲批上市將進一步提升曲妥珠單抗在國內的可及性,強化HER2陽性乳腺癌及胃癌患者的規范化治療。
國內審評審批·新受理
本周CDE新增報生產受理號18個,共15個品種,更多動態見下表:
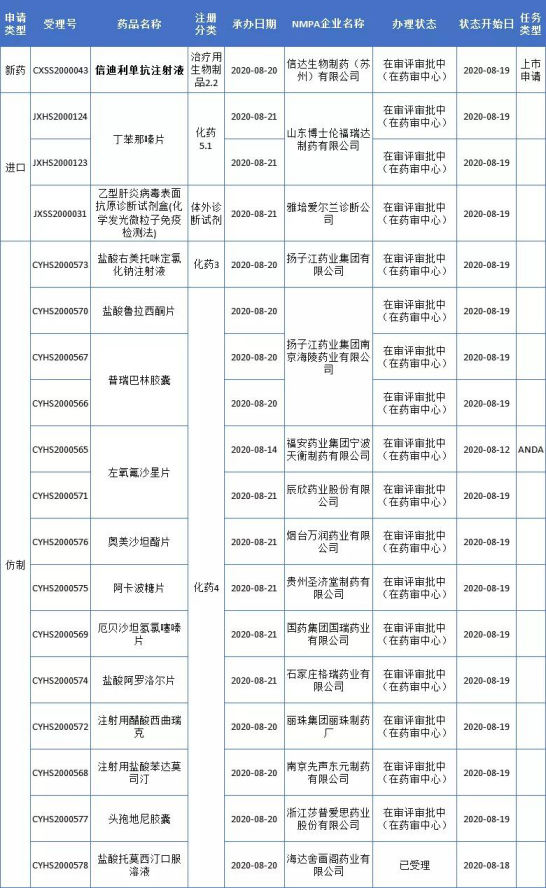
信迪利單抗新適應癥上市申請獲受理
近日,NMPA受理了達伯舒?(信迪利單抗注射液)與吉西他濱聯合用于治療一線鱗狀非小細胞肺癌患者的新適應癥上市申請。在此之前,NMPA已于2020年4月23日正式受理達伯舒?(信迪利單抗注射液)用于非鱗狀NSCLC一線治療的新適應癥申請。信迪利單抗注射液獲批的第一個適應癥是復發/難治性經典型霍奇金淋巴瘤,并入選2019版中國臨床腫瘤學會(CSCO)淋巴瘤診療指南。2019年醫保國談中,達伯舒?(信迪利單抗注射液)是唯一進入國家醫保的PD-1抑制劑。
數據來源:藥智數據、企業公告等網絡公開數據
信息來源:藥智網、企業公告等網絡公開信息
聲明:本文系藥智網整合內容,不代表本平臺觀點。如涉及作品內容、版權和其它問題,請與本公眾號留言聯系,我們將在第一時間刪除內容。
