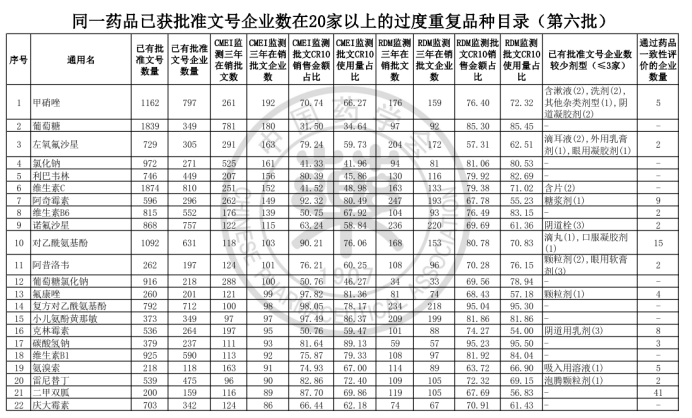
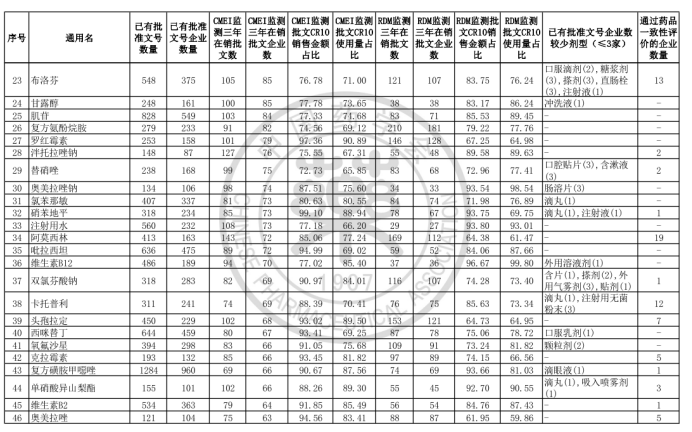
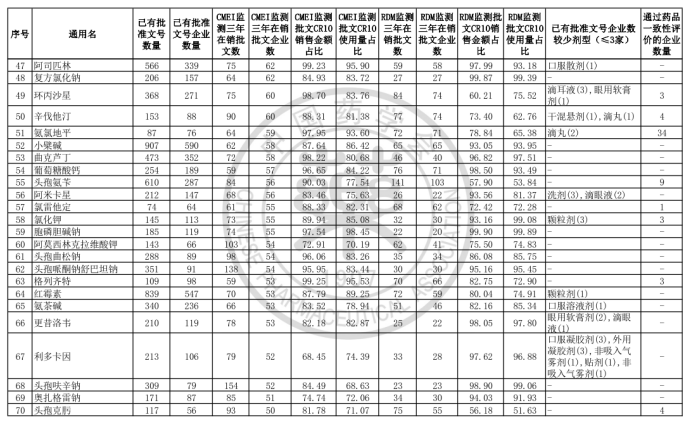
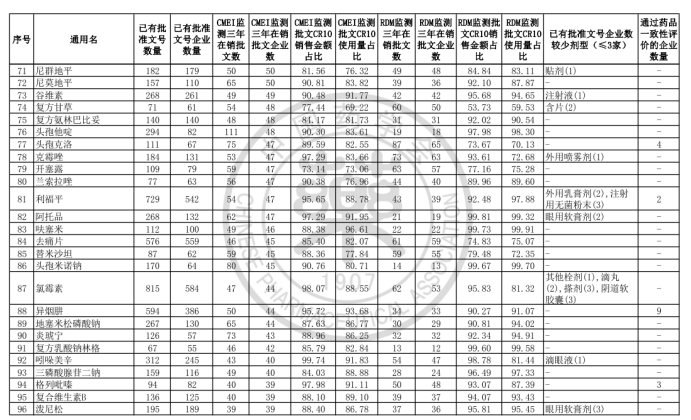
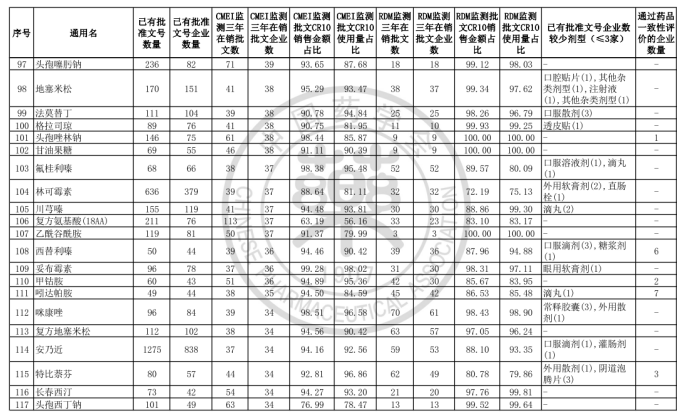
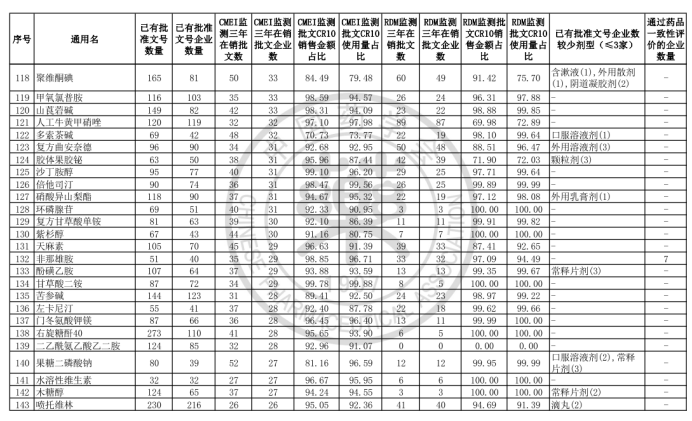
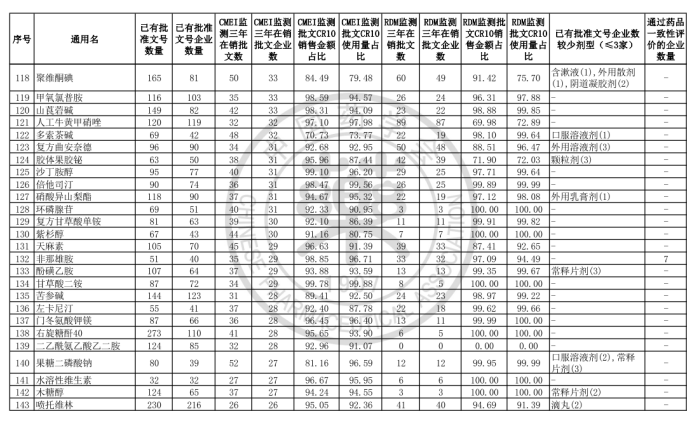
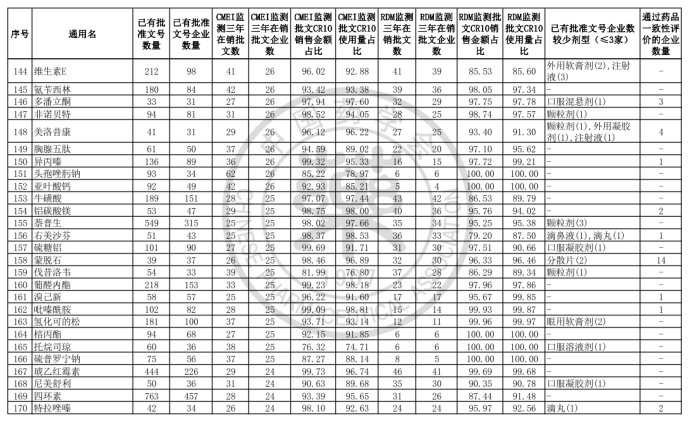
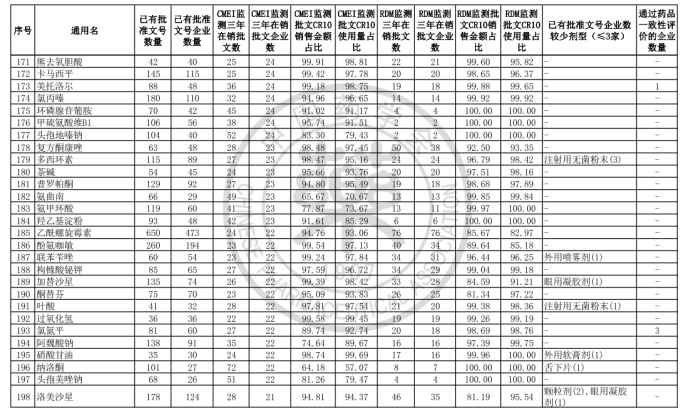
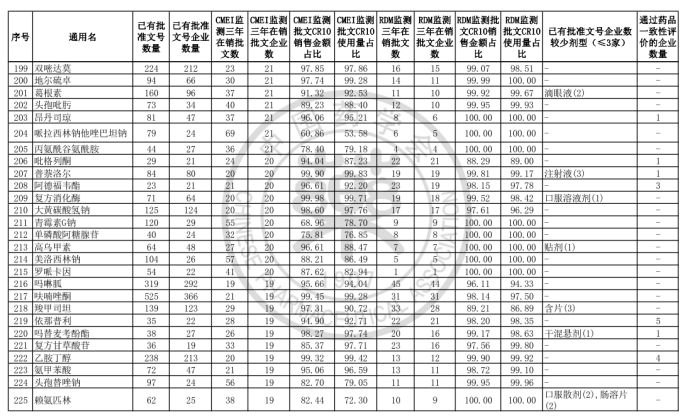
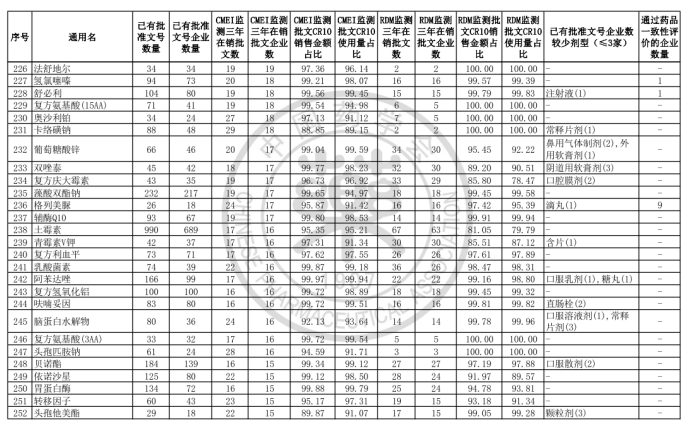
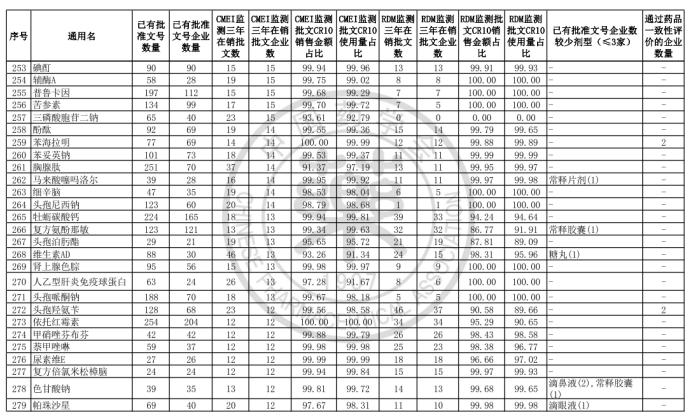
中國藥學會發布《關于發布第六批過度重復藥品提示信息的公告》,公布了《同一藥品已獲批準文號企業數在20家以上的過度重復品種目錄(第六批)》。
根據公告顯示,該目錄是中國藥學會和國家藥品監督管理局信息中心、南方醫藥經濟研究所共同協作,對已獲批上市藥品在2017-2019年間的銷售情況進行監測分析,形成第六批過度重復藥品提示信息目錄,共302個過度重復品種,涉及臨床藥理學和治療學分類的14個大類、60個亞類,與《關于發布第五批過度重復藥品提示信息的公告》發布的過度重復品種目錄相比,調出1個品種;目錄提示信息新增兩項數據內容,一是基于中國上市藥品目錄集對通過仿制藥質量和療效一致性評價的企業數量進行標注;二是基于藥品已有批文數據庫,對已有批文企業數≤3的劑型進行標注。自2014年9月原國家食藥監總局公布《第一批過度重復藥品品種目錄》,目前已是第六批。梳理公布的目錄發現,過度重復藥品已經有大量企業生產或正在申報投產,市場需求已經飽和或者接近飽和。
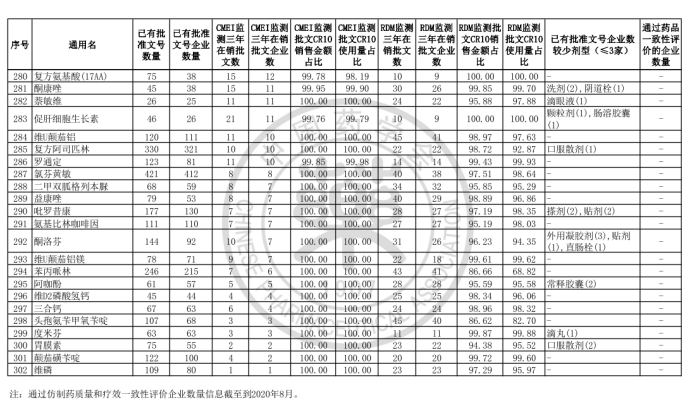
據藥智網梳理發現,有4個品種擁有批文數超過1000條,其中最多的為維生素C,已有批準文數1874條,涉及企業高達810家;其次是甲硝唑,已有批準文數1162條,擁有批準文號數的企業達797家,在售該品種的企業更是有192家,是第六批過度重復藥品在銷企業最多的品種,另CMEI監測顯示甲硝唑市場銷售額最高的10個產品,已占據市場份額的70.74%。
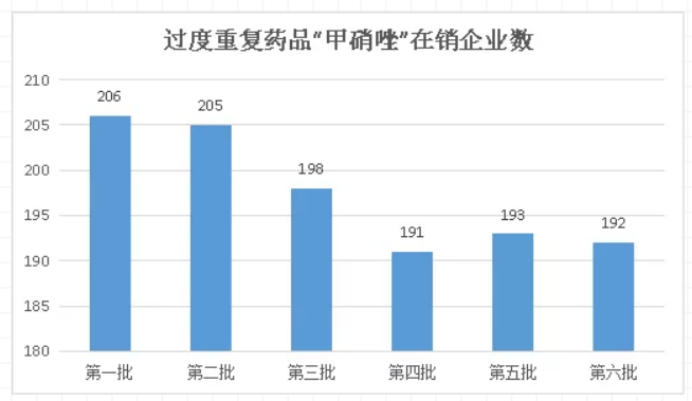
另外值得注意的是自第一批過度重復藥藥品目錄公布以來,甲硝唑在銷企業數由第一批的206家企業下降至現在的192家。第六批過度藥品重復目錄顯示,甲硝唑目前已有5家企業通過一致性評價,且值得提及的是甲硝唑片為第二批集采目錄藥品,遠大醫藥和四川科倫藥業分別以5.07元/盒和1.84元/盒中標。
公告顯示,發布過度重復藥品目錄是提醒相關藥品生產企業和研發機構,應充分了解市場供需狀況,科學評估藥品研發風險,慎重進行投資經營決策。建議各省、自治區、直轄市藥品監督管理部門加強對企業的指導,對已經公布的過度重復藥品提示信息,主動做好宣傳工作,引導企業理性研發和生產。
醫藥經濟報曾發文中,有市場人士認為,“由于企業研發是自主行為,決策時要考慮市場、供應和創新方向等多重因素,并承擔相應風險。同類研發也存在一致性問題,如涉及到參比間的比較、工藝一致性、處方一致性等問題,某一品種是否值得研發、申報、生產以及上市后還要面臨哪些市場考驗,都需要企業自行評估。”
另,從已公布的目錄來看,目前很多品種已經高度飽和,并不適合繼續申報新的批文,尤其是普藥,例如氨氯地平片、阿莫西林膠囊等,競爭極其激烈,并且氨氯平片有34家通過一致性評價,阿莫西林有19家通過一致性評價。在集中采購逐漸常態化之下,低質量不具競爭的仿制藥逐漸被淘汰,過度重復藥品目錄的發布,有力的幫助了企業決策,同時從行政手段來限制藥企的申報,為先獲得批文的生產廠家制造了競爭壁壘。一些不具市場競爭的企業,很可能會逐漸被市場淘汰,最終注銷批文。從另一方便來看或將有效的提升了藥品的質量,做到質優價廉,保障了資源的合理利用,又福利了患者。
附名單: